A melanomák a bőrben található, fekete-barna festékanyagot – idegen szóval pigmentet – termelő sejtekből, a melanocitákból fejlődhetnek ki. Melanomára utalhat, ha megváltozik egy anyajegy színe, pigmentációja, felszíne vagy alakja. Melanomát jelezhet az is, ha megváltozik egy anyajegy határa, emellett terjedni, növekedni kezd a bőrfelszínen. Magyarországon évente csaknem 2000-re tehető az újonnan felismert melanómás betegek száma, és csaknem 400-an halnak meg a betegségben.
A melanoma tünetei
Melyek azok az anyajegyen történő változások, amelyek melanoma kialakulására utalhatnak?
- Megváltozik a színe, a festékezettség (pigmentáció) egyenetlen lesz: különféle árnyalatú barna és/vagy fekete keveredhet pirosas, fehéres, kékes, szürkés, vagy rózsaszínű árnyalatokkal
- Megváltozik a felszíne, kiemelkedik a bőrből, göbössé válik, megvastagodik
- Az anyajegy alakja aszimmetrikussá válik, vagy egy új aszimmetrikus anyajegy jelenik meg
- Megváltozik a határa, terjedni, nőni kezd a bőrfelszínen. Esetleg kisebb anyajegy jelenik meg a régi mellett, amelyek esetleg egymásba is átmosódnak
- Kisebbedik, felmaródik vagy kifekélyesedik
- Vérezni kezd
Fontos megemlíteni, hogy a melanoma nem bőrrák, a bőrrák ugyanis nem a fekete-barna festékanyagot termelő melanocitákból, hanem a bőr saját hámsejtjeiből indul ki.
A melanoma diagnózisa
A melanoma szűrése egy konzultációval kezdődik, amelynek része a kórelőzmény felvétele, a napozási és fényvédelmi szokások, illetve az aktuális panaszok kikérdezése.
A bőrelváltozások szemmel történő, alapos szakorvosi vizsgálata dermatoszkópos vizsgálattal egészül ki.
A vizsgálatot végző szakorvosnak a bőrelváltozások és az anyajegyek formája, szabályossága, szélei, a bőrből való előemelkedésük, pigmentszerkezetük és erezett voltuk ad nagyon sok információt. Az anyajegyek helye és jellege is fontos: meg kell állapítani, hogy ki vannak-e téve sérülés- és irritációveszélynek, illetve – pigmentszerkezetük révén – magukban hordozzák-e a rosszindulatú átalakulás lehetőségét.
A rosszindulatú elváltozások ezzel a módszerrel már egészen korán és megbízhatóan kiszűrhetők, és akár teljes mértékben gyógyíthatók is. A melanomák esetében fontos, hogy nem a daganat felszíni, hanem a mélységi kiterjedése a lényeges: ha a tumort egy milliméternél kisebb mélységnél sikerül eltávolítani, akkor elégséges lehet egy egyszerű kimetszés is, ami végleges gyógyuláshoz vezethet. A szemmel és dermatoszkóppal végzett szűrés egyértelmű választ ad arra, hogy szükség van-e a gyanúsnak ítélt bőrelváltozások eltávolítására.
A vizsgálatot a szövettan teszi teljessé, amellyel teljes biztonsággal meghatározható a sejtek rossz-, avagy jóindulatúsága.
A melanoma stádiumbeosztása
Kezdeti stádiumában a daganat még csak a bőr felső rétegében, a hámban van jelen – ez a helyben növekvő, úgynevezett in situ stádium. A páciens ekkor még egy egyszerű kimetszéssel is teljesen gyógyítható.
Amikor a melanoma már a bőr mélyebb rétegeibe is átterjed – ahol már nyirok- és vérerek is vannak – onnantól kezdve megnő az áttétek kialakulásának esélye, mivel a sejtek – az erek útján – már a távolabbi szervekbe (májba, tüdőbe, agyba, csontokba, stb.) is átkerülhetnek, majd ott megtelepedve nőni kezdenek, és tönkretehetik az adott szervek működését.
I-es és II-es stádiumú melanomák
- Tis stádium: helyben növekvő (in situ), a bőr epidermisz nevű rétegében maradó nem invazív daganat
- T1a stádium: a tumor invazív (vagyis az epidermiszen kívül bőr egyéb rétegeibe is elkezdett átterjedni), mérete azonban még csak 1 milliméteres vagy ennél kisebb
- T1b stádium: a még mindig csak 1 milliméteres vagy ennél kisebb tumor már fekélyesedést is mutat
- T2a stádium: a tumor mérete 1 és 2 milliméter közötti, fekélyesedés nélkül
- T2b stádium: a tumor mérete 1 és 2 milliméter közötti, fekélyesedéssel
- T3a stádium: a tumor mérete 2 és 4 milliméter közötti, fekélyesedés nélkül
- T3b stádium: a tumor mérete 2 és 4 milliméter közötti, fekélyesedéssel
- T4a stádium: a tumor mérete meghaladja a 4 milliméteres vastagságot, fekélyesedés nélkül
- T4b stádium: a tumor mérete meghaladja a 4 milliméteres átmérőt, fekélyesedéssel
III-as stádiumú melanoma
Abban az esetben, ha a melanoma elérte a III-as stádiumot, a tumor vastagságát már nem veszik figyelembe a stádium besorolásánál. A kifekélyesedés (kisebesedés vagy idegen szóval ulceráció) mikroszkóp alatt megállapítható mértéke ezzel szemben továbbra is szerepet játszik a daganat súlyosságának megítélésében, hiszen ennek fontos szerepe van a betegség későbbi kórlefolyása (progressziója) szempontjából.
A III-as stádiumú tumorok már elérték a nyirokcsomókat, illetve a közeli nyirokcsomók és az elsődleges tumor között elhelyezkedő szöveteket. Ezek tehát már áttétet is adó melanomák, amelyeket az őrszem-nyirokcsomóból vett szövetmintával diagnosztizálnak (az őrszem-nyirokcsomó a tumorhoz legközelebb eső nyirokcsomót jelenti). Az őrszem-nyirokcsomóból abban az esetben szokás mintát venni, ha a tumor vastagsága már meghaladta az 1 millimétert, vagy ha egy ennél vékonyabb melanoma már a fekélyesedés jeleit mutatja a mikroszkópos felvételeken.
Legújabban már azokat a melanomákat is III-as stádiumúnak tekintik, amelyek rendkívül kis méretű, kizárólag mikroszkóp alatt észrevehető áttéteket, úgynevezett mikrometasztázisokat tartalmaznak. Az, hogy a tumor mennyire tekinthető előrehaladottnak a III-as stádimon belül (ezt az N betű – Nódus, vagyis nyirokcsomó – és az utána írt, 0-4-ig terjedő szám mutatja meg, vagyis hogy a tumor milyen szinten terjedt át a közeli vagy távolabbi nyirokcsomókba), több faktortól is függ. Ezen faktorok közé tartozik például, hogy az áttétek még épp csak terjedőben vannak, vagy már el is érték a nyirokcsomókat, hogy mennyi, már áttétes nyirokcsomó van jelen, ezekben mennyi daganatsejt található, illetve hogy ezek az áttétek mikrometasztázisok-e, vagy épp szabad szemmel is láthatóak.
IV-es stádiumú melanomák
Ebbe a csoportba azok a melanomák tartoznak, amelyek már nemcsak az elsődleges tumorhoz közel eső, hanem a távoli nyirokcsomókba vagy a belső szervekbe is áttéte(ke)t adtak. A melanomák leggyakrabban a tüdőkbe adnak áttétet, ezt követően pedig a májba, az agyba, a csontokba és az emésztőszervrendszerbe (gyomor, vékonybél, vastagbél, végbél).
A IV-es stádiumú melanomák súlyosságát az M betűvel és az utána írt, 0-4-ig terjedő számmal határozzák meg, azt is figyelembe véve, hogy az áttét(ek) mely szerve(ke)t érintik. Mindezeken kívül a szérum laktát dehidrogenáz (LDH) nevű enzim szintje is meghatározásra kerül (emelkedett vagy normális-e az enzimszint?)
A melanoma okai
- A melanoma kialakulásában a napsugárzásnak való kitettség mértéke a legfontosabb kockázati tényező: különösen megnő a kockázat leégések (főképp a többszöri és hólyagos leégés) miatt. A gyermek- és kamaszkorban elszenvedett sorozatos (háromnál több) komoly leégés megduplázza a felnőttkori melanoma kialakulásának kockázatát. Különösen veszélyes az UV-sugárzásnak (természetes és mesterséges egyaránt) való kitettség.
- A másik fontos faktor a bőr típusa. A nagyon fehér bőr fokozott kockázatot jelent. (Az eredendően sok pigmenttel rendelkező, azaz sötét bőrű rasszok esetén a melanoma jóval ritkábban fordul elő.) Azoknál a fehér bőrű embereknél, akik gyorsan lebarnulnak, szintén ritkábban alakul ki ez a daganat.
- Fokozott kockázatot jelentenek az anyajegyek is (bár az esetek 70%-ában a daganat újonnan alakul ki, és nem köthető a korábban is már meglévő anyajegyhez.) A szabálytalan anyajegyek jelenléte megnövekedett kockázatot jelent.
- Fontos megemlíteni, hogy akiknél korábban úgynevezett bazalioma (egy áttétet szinte soha nem okozó bőrráktípus) alakult ki, ők ugyancsak fokozottabb melanoma-kockázatnak vannak kitéve.
- A melanoma kialakulásának esélyét a családi halmozódás is jelentősen fokozhatja (az elsőfokú rokonnál történt előfordulás több mint kétszer nagyobb kockázatot jelent).
- Egy tovább kockázati tényező az egyén élete során alkalmazott tartós immunszupresszió (az immunrendszer elnyomása) is.
Szerzett mutációk
A melanomákat korábban a tumor eredete, szövettana és anatómiája szerint sorolták be különféle alcsoportokba, ma már azonban azon irányító (driver) mutációk szerint kerülnek besorolásra a daganatok, amelyek a leginkább felelőssé tehetőek a daganat kialakulásáért. (Az irányító mutációk csoportjába a genetikai állomány olyan módosulásait soroljuk, amelyek növekedési előnnyel ruházzák fel a sejteket, ezért előnyös kiválasztódás hat rájuk. Az irányító mutációk tehát aktívan részt vesznek a rosszindulatú tumorok kifejlődésében [onkogenezis]).
A melanoma esetében ezen irányító mutációk közé tartoznak
- a BRAF (a melanomák 37-50%-a)
- a GNA11 (a melanomák 1,2%-a)
- a GNAQ (a melanomák 1,3%-a)
- a KIT (a melanomák 2-8%-a)
- a MEK1 (MAP2K1) (a melanomák 6-7%-a)
- és az NRAS (a melanomák 13-25%-a)
nevű onkogénekben visszatérően előforduló mutációk. (Az onkogének olyan gének kóros változatai, amelyek normális esetben a megfelelő ütemű sejtosztódást, a normális sejtciklust szabályozzák [normális alakjukban e géneket protoonkogéneknek nevezik]).
A BRAF, a GNA11, a GNAQ, a KIT, a MEK1 (MAP2K1) és az NRAS mutációi az összes melanoma nagyjából 70 százalékában fordul elő.
Az említett onkogéneken kívül a CTNNB1 génben megjelenő mutációk szerepét ugyancsak leírták a melanomák kialakulásában (a melanomák 2-4%-a).
Öröklött mutációk
A melanomáknak létezik egy olyan formája is, ami családi halmozódást mutat és öröklött mutációk miatt alakul ki. Ezek a mutációk – az életünk során felhalmozódó, szerzett mutációkkal ellentétben – a szervezet összes sejtjében jelen vannak.
Az öröklött melanomák esetében a családban jellemzően 2 vagy ennél több elsőfokú rokonnál (például a szülők, testvérek és/vagy gyermek) fordul elő melanoma. Az öröklődő forma nem túlságosan gyakori: az újonnan diagnosztizált melanomás esetek mindössze 8%-ánál van jelen a melanoma a közeli rokonok valamelyikénél, és ennél is ritkábban – mindössze 1-2%-ban – adódnak olyan esetek, amikor a betegség 2 vagy ennél több közeli rokonnál is jelen van.
A melanoma családi halmozódású eseteiben gyakran fordulnak elő az atipikus vagy másnéven diszplasztikus névuszok: ezek veleszületett anyajegyek, amelyeknek a széle általában szabálytalan és kevésbé élesen határolódik el a környezetétől, emellett az alakjuk is szabálytalan (nem ovális vagy kerek). Az atipikus anyajegyek pigmentációja változó jellegű az anyajegyen belül. Az atípusos anyajegyeket muszáj nagyon szigorúan ellenőrizni: az anyajegy méretében, alakjában vagy színében bekövetkező bármilyen változás azt jelezheti, hogy megkezdődött az anyajegy rosszindulatúvá válásának folyamata.
A melanoma családi halmozódású esetei többnyire az érintettek 30-as életéveiben kerülnek diagnosztizálásra, szemben az élet során felhalmozódó, szerzett mutációk miatt kialakuló esetekkel, amelyek átlagosan csak az 50-es életévek környékén jelennek meg az általános népességen belül.
Az örökletes melanomák hátterében mostanáig két gén, a CDKN2A és a CDK4 mutációit sikerült kimutatni: a betegség nem minden esetben fog kialakulni akkor sem, ha az öröklődő mutációk jelen vannak ezekben a génekben, a fiatalabb korban kialakuló melanoma kockázata azonban jelentősen megnövekszik. A kétféle gént érintő mutációk csak az öröklődő melanomák egy kisebb százalékáért felelősek; az egyelőre még nem ismert, hogy az örökletes melanomák többi esetéért mely gének mely mutációi felelősek. A CDKN2A-n és a CDK4-en kívül az MC1R gén különféle variánsait is összefüggésbe hozták a melanoma kockázatnövekedésével. Ez a gén a bőr pigmenttartalmának szabályzásában játszik szerepet.
A melanoma kezelése a korai stádiumban főként a sebészeti eltávolítást» jelenti, mely sok esetben teljes gyógyuláshoz vezet. Ha a tumor még nem terjedt át a regionális (a környezetében lévő) nyirokcsomókra, akkor igen jók a beteg gyógyulási esélyei (95%-os túlélési arány 5 évvel a diagnózis után).
- A műtét teljes gyógyulást eredményező lehet akkor is, amennyiben a melanoma már átterjedt a regionális nyirokcsomóra. A távoli szervekbe adott áttétek esetén azonban az 5 éves túlélési arány már jóval alacsonyabb.
- A sugárkezelés hasznos lehet a helyileg panaszt okozó áttétek ellátásában, a műtét kiegészítéseként. Különösen fontos az agyi áttétek kezelésében, az esetleges agyműtétek után visszamaradt tumorszövetek elpusztításában. Agyi áttétek esetén végzett sugárterápia lehetővé teszi az életminőség javítását, illetve az alkalmazott szteroidok mennyiségének csökkentését.
- A sugárkezeléssel egy időben adott citosztatikus kezelés (kemoterápia) tovább fokozhatja a terápiás hatást.
- A melanomával kapcsolatban számos új eljárás klinikai próbái folynak: a páciens saját tumorsejtjeiből készített vakcinákkal, új kemoterápiás és immunoterápiás eljárásokkal és ezek kombinációival, illetve új sebészeti technikákkal. A végtagokon kifejlődött melanomák esetében próbálták ki az elszigetelt, nagy dózisú kemoterápiát: a páciensek érintett végtagjainak vérkeringését átmenetileg elszigetelték a test többi részének keringésétől, így nagy mennyiségű kemoterápiás szerrel kezelhették a daganatot, mert annak káros hatása nem terjedt ki a teljes szervezetre.
Áttörő eredmények a melanoma kezelésében immunterápiával
2011-ben két olyan rákgyógyszer is törzskönyvezésre került, amelyekkel már a melanoma előrehaladott formáiban is ígéretes eredményeket lehet elérni. Ezek egyike ráadásul egy olyan megközelítésen alapul, ami teljesen újszerűnek tekinthető a rákgyógyításban: az immuno-onkológiának nevezett tudományterület fő célja, hogy olyan rákgyógyszerek kerüljenek kifejlesztésre, amelyek nem közvetlenül támadják a daganatot, hanem a beteg saját immunrendszerének segítségével győzik le azt. A melanoma elleni új immunterápiás szer azoknál a betegeknél is alkalmazható, akiknél a daganatsejtek fehérjéit gátló célzott kezelés a gyógyszerhatékonysághoz szükséges mutációk hiánya miatt egyáltalán nem jöhet szóba.
Az áttétes melanomák kezelésének jövőjét a kombinált terápiák jelentik
Egy 2013-as klinikai vizsgálati eredmény szerint két immunterápiás készítmény (ipilimumab és nivolumab) hatékonysága együtt, egy időben alkalmazva 53%-os objektív válaszarányt eredményezett a legmagasabb dózist kapó 17 beteg körében. (Az objektív válaszarány – Objective Response Rate, rövidítve ORR – a klinikai vizsgálatok egyik úgynevezett végpontja, vagyis olyan jelzőszáma, amellyel a vizsgált gyógyszer hatékonyságát mérik. A klinikai vizsgálatok későbbi fázisaiban már inkább a teljes túlélést, a progressziómentes túlélést, esetleg az életminőség általános javulását használják elsődleges mérőszámként).
Összehasonlításul: a két szer – külön-külön alkalmazva – korábban 11, illetve 41%-os objektív válaszarányt eredményezett, az onkológusok pedig már a 41%-os értéket is valódi áttörésként értékelték.
Hogyan hatnak az immunterápiás szerek?
A két immunterápiás szer közül az első (ipilimumab) a segítő (helper) T-sejtek felszínén található CTLA-4-et gátolja.
A másik szer (nivolumab) a programozott sejthalállal összefüggő jelfogó molekulát, az úgynevezett PD-1-et célozza meg, amely – az immunrendszer egyéb sejtjei mellett – szintén a T-sejtek felszínén van jelen. Mindkét gyógyszer a szervezet melanoma elleni, természetesen is meglévő harcképességét erősíti fel azáltal, hogy az immunsejtekre hat.
Szintén a programozott sejthalállal összefüggő jelfogó molekulát, a PD-1-et gátolja a lambrolizumab nevű antitest.
Célzott terápiák
A BRAF gén mutáns változatainak a melanoma kialakulásában betöltött szerepét 2002-ben azonosították. A BRAF mutációi a melanomák körülbelül 40 százalékánál játszanak szerepet a daganat korai növekedésében és túlélésében: a mutációk hatására fokozódik a BRAF fehérje aktivitása, ennek következtében pedig a jelátviteli útban utána következő MEK és ERK fehérjék aktivitása is növekedni kezd.
A BRAF gént érintő mutációk nagyjából 90 százaléka ugyanott, a V600E jelzésű ponton jelentkezik: a gén által kódolt fehérjében ilyenkor egy aminosavcsere történik, aminek hatására a BRAF „süketté válik" azokra a jelekre, amelyek normális esetben megakadályozzák a fehérje túlzott aktivitását.
A kezelés új standardja a BRAF és a MEK kombinált gátlása lehet
Az Európai Klinikai Onkológiai Társaság 2014-es kongresszusán mutatták be azt a két új klinikai vizsgálatot, amelyekből az elsőben egy már jól ismert BRAF-gátló gyógyszert kombináltak egy még kísérleti fázisban lévő MEK-gátlóval, a másodikban pedig egy újabb típusú BRAF-gátlót és egy az USA-ban már törzskönyvezett MEK-gátló gyógyszert adtak a betegeknek.
Mindkét klinikai vizsgálat eredménye megerősíti, hogy a kombinált célzott kezelés egyértelműen hatékonyabb annál, mintha a betegek kizárólag BRAF-gátlót kapnának.
Az optimális kezelést megalapozó mutáció vizsgálatok
A rosszindulatú festékes anyajegy-daganatok (melanomák) esetén az összes jelentősebb mutáció vizsgálatát lehetővé teszi a panel, ezek segítségével a betegek számára leginkább előnyös célzott terápiák választhatók:
- A BRAF mutáció jelenléte a BRAF gátlószerekkel szembeni érzékenységre utal.
- Az NRAS mutáció negatív prognosztikai faktor, illetve a BRAF gátlószerekkel szembeni ellenálló-képesség kialakulásának egyik lehetséges oka. NRAS mutáns melanomákban hatékonynak bizonyultak a MEK gátlószerek.
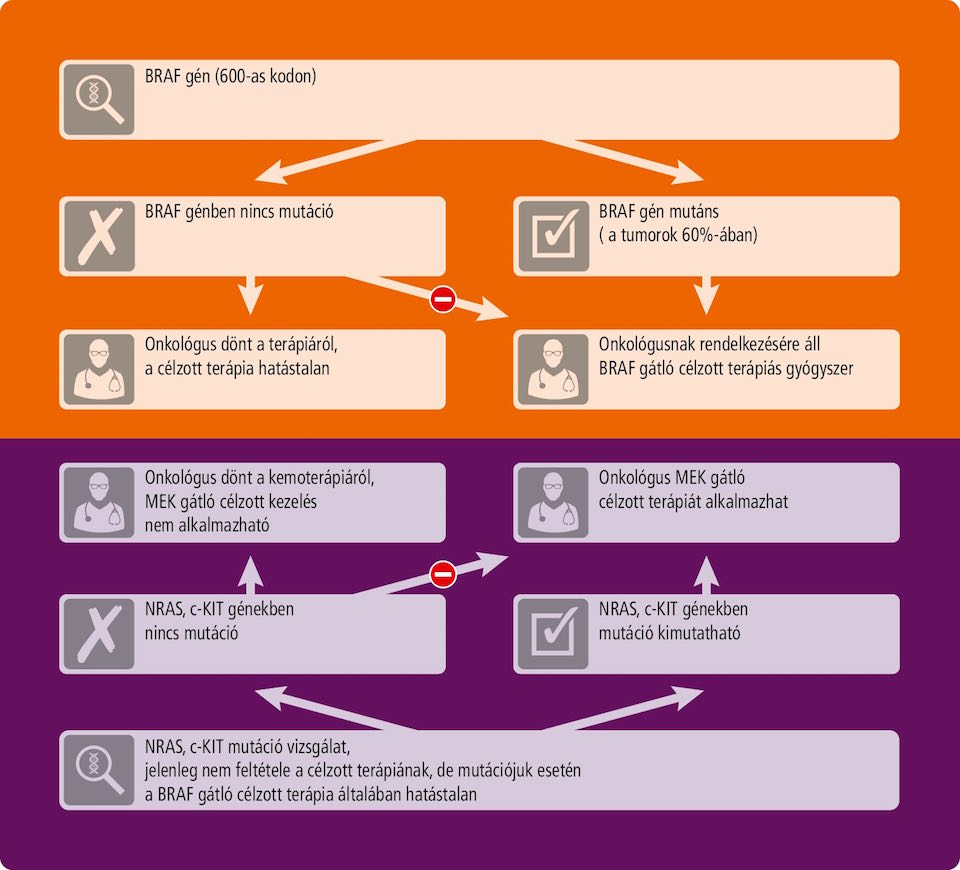
A jelenleg alkalmazott terápiák és a melanoma mutációk összefüggéseit ez az ábra szemlélteti.